本文简要介绍了内镜活检和内镜切除标本的处理以及相关的病理知识,从病理医生的角度给内镜医生提出建议,比较适合初学者。
为了方便读者理解,补充了相关的病例和病理图片,这些图片均来源于首都医科大学附属北京友谊医院病理科,感谢陈光勇主任的团队。
(摘自:消化器内视镜 Vol 29 No.3 2017 369-375 作者:河内洋 藤崎順子 癌研有明医院)
01
活检标本的处理
1、活检标本、钳除标本的处理
以诊断为目的的活检标本、大肠息肉钳除的病理标本,在标本取材或切除后要快速放入福尔马林溶液中固定,如果标本在室温长时间放置,会造成标本干燥,组织变性。从而造成标本质量下降,影响病理学诊断。
标本固定时间建议在24小时以内。固定时间过长或过短都会影响免疫组化染色的结果。对于胃癌,HER2等分子检测的重要性日益受到关注。因此,良好的标本处理更加重要。
2、内镜切除标本的处理
平坦病变、内镜下黏膜切除术(EMR)、内镜下黏膜剥离术(ESD)的标本,在放入福尔马林液之前,应当先进行标本的延展固定。
标本应放在泡沫板或是橡胶板上,病变的黏膜面向上,在边缘部用固定针使标本适度伸展进行固定。
当用固定针固定标本的边缘时,要注意避免标本破损。另外,为了防止标本向一侧皱缩,应均匀地使标本伸展。最好在标本固定时,与充气量充足的内镜下图像进行比对,固定成相似的形状,方便日后内镜图像和病理所见进行对比。
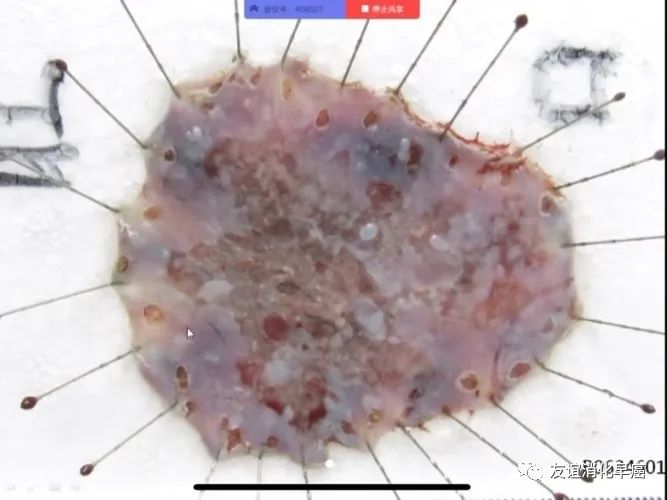
标本展开固定
对于分次切除的标本,要了解分次切除的各部分的位置关系,才能准确进行固定。固定良好的标本有利于病理医生制作组织标本,准确判断病变浸润深度以及断端,并对肉眼所见和组织学所见,内镜所见和病理所见进行比对。
不同单位,由于人手以及设备的问题,标本固定这项工作有时并不能顺利进行,但是我们应当理解,这项工作对于准确的病理学诊断至关重要。另外,大肠的有蒂和亚蒂息肉样病变,不需要把标本延展固定。
包含食管、食管胃结合部的鳞状上皮的标本,要进行碘染色。碘染色时使用内镜检查中所用的碘液染色,染色后要进行拍照,以便与内镜图像进行对比。
标本固定后要尽快放入福尔马林液中进行组织固定。如放置过长会导致组织变性,影响诊断。福尔马林液要充分浸泡病变,如浸泡不充分,会造成标本固定不良或标本干燥。切除的标本,如果使用内镜或解剖显微镜进行观察时,要注意尽可能缩短观察时间,以防止标本干燥。
为了防止标本干燥,福尔马林液固定前的新鲜标本,可以使用生理盐水浸泡,切忌不要擦拭黏膜表面。若擦拭新鲜标本,可能会造成黏膜上皮的脱落,影响诊断。若是为了内镜图像和病理图像对比,而造成标本表面信息缺失,就本末倒置了。固定后的标本同样要注意避免擦拭标本表面,破坏标本。
把标本送到病理科时,应当在申请单中提供以下信息。
1. 治疗前的病变范围,浸润深度,是否合并溃疡。
2. 活检结果(组织类型等)。
3. 标本方向,如哪边是口侧。
4. 病变的位置。
5. 靠近断端的部位等。也应指出治疗前内镜观察时特别关心的区域。
3、由于标记所造成的标本热变性
在ESD时,全周切开前,为了确定切除范围,需要先进行标记。另外,近年来,为了确定内镜下的病变范围,也有人在病变的周围进行标记,由于标记时组织标本灼烧会导致组织变性,使细胞核、细胞以及腺管形态发生改变。确定切除范围所进行的标记,通常是在病变的外侧,一般影响不大。
但是,如果在病变的边界或是病变内部进行标记的话,有时会造成该部位的组织学评价困难。病理图像与内镜图像对比固然重要,但是如果干扰了病理学评价,就本末倒置了。这时,内镜医生应与病理医生进行沟通,采取恰当的办法。
4、切割
内镜切除标本的切割通常是由病理医生完成的。也有的医院是由内镜医生进行该项操作。
由病理医生切割标本时,需要向病理医生提供标本的相关信息,这对诊断至关重要。标本的切割一般是间隔2~3mm。有蒂的病变则经蒂部进行切割。有时候要对标本蜡块进行深切,这时,切割线应与想观察的部位稍微离开一点距离,这样有利于进行薄切。
对于大肠的绒毛状腺瘤、颗粒型侧向发育型肿瘤,特别是病变较大时,间隔2~3mm进行切割,有时存在困难,这时候可以切的稍微厚一点。对于内镜下怀疑有浸润的部位,要特别注意,合理地设定切割线。切割标本后,要对有切割线的标本进行拍照。
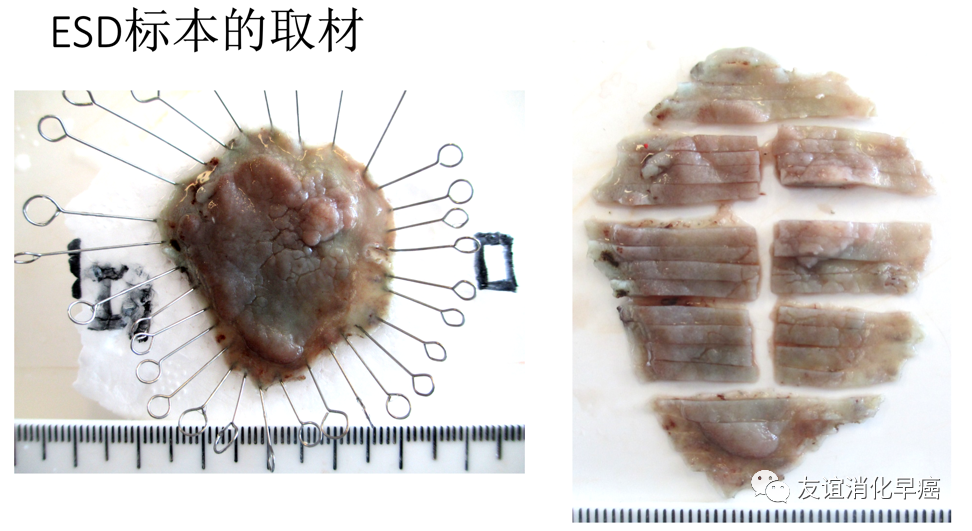
包含鳞状上皮的食管和食管胃结合部的标本,要进行碘染色。为了取得更好的染色效果,要充分冲洗标本上的福尔马林固定液,一般不低于60min,建议采用流水冲洗。一般选用低浓度碘液0.1%~0.5%,反应时间1min左右,这样可以得到较好的对比效果。
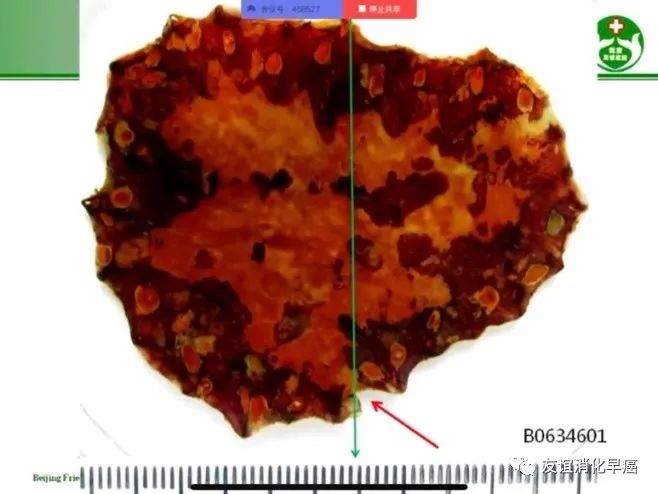
食管病变标本碘染色
02
内镜医生应知道的病理学知识
1. 活检标本病理学诊断应注意的问题
对活检钳钳取的病理标本进行病理诊断时,所能观察到的标本一般很小。病理组织通常是在怀疑有问题的病变部位进行取材,这样才能够获得准确诊断。为此,怀疑为癌的标本,如果标本过小的话,就不能进行准确诊断。
在炎症和肿瘤鉴别时,有时也会遇到鉴别困难的异型腺管,这时需要对标本进行深切或免疫组化染色。有时,即便通过这样的方法,还不能确定诊断。
另外,有时内镜下诊断为恶性肿瘤而活检取材,病理诊断为非肿瘤性病变或良性病变的情况也是存在的。
当内镜诊断与病理诊断偏离时,要和病理医生进行充分沟通。内镜下进行再评估,再活检、动态观察后复查。
溃疡性结肠炎、克罗恩病等炎性肠病,仅通过病理学并不能确诊,应当综合包含内镜在内的临床所见来获取诊断。不过,病理学上所观察到的炎症分布以及类型对诊断也是有帮助的。活检取材时,不仅要对炎症部位进行取材,也要对正常部位取活检,如果能发现轻微的炎症、肉芽肿、既往炎症改变,对诊断也是有用的。
一般来说,活检取材部位是在有组织结构的部位,但是,也有例外。比如,阿米巴痢疾时,有白苔的部位多能找到滋养体,这时建议在白苔较多的部位进行取材。有时也要针对需要鉴别诊断的疾病进行取材,这对诊断是有帮助的。
2、 内镜切除标本的病理诊断需要注意的基本事项和要点
1)切除断端
切除断端分为水平断端和垂直断端。相当于各种黏膜的切割线和黏膜下层侧的切割面。
根据处理规约一般用HM(horizontal margin)代表水平断端,VM(vertical margin)代表垂直断端。
水平断端阳性(HM1)时,表示有黏膜内癌(上皮内癌)残留。但是,如果沿着病变边缘设定切割线时,病变边缘由于组织灼烧、热变性会造成组织缺失,但是,实际上并无病变残留,这种情况其实并不少见。病理报HM1时,建议对病变部位动态观察,确定有无残留。
垂直断端阳性(VM1)时,代表在垂直切面存在黏膜下层深层浸润。表示浸润深度达到粘膜下层或以深,不仅可能有局部残留,还有淋巴结转移的风险,需要讨论是否追加外科手术。
标本的水平断端、垂直断端判定困难时,记为“HMX”和“VMX”,这也有各种不同情况。HMX时,标本切缘由于热变性,判断困难,这时应根据内镜下的病变范围,治疗时设定的切缘、组织学图像等综合判断,明确是否有病变残留。临床和病理之间要进行充分讨论。建议在设定边缘切割线时,为了避免边缘灼烧所致的组织变性,应包含部分非肿瘤组织。
评价深部断端时,热变性的部分,由于血管、炎性细胞、纤维肉芽细胞密集,有时会判断困难,记为VMX。另外,由于有间质存在,断端附近的癌灶不连续,即便没有见到癌灶,也不能否定有病变残留。这种病变,大多存在粘膜下层深浸润癌,应参考其他所见判断是否需要追加治疗。
息肉切除时,如果切除的标本过小,有时也可能无法判断深层断端。
即便是黏膜内癌,有时也可能会判断为VMX。ESD行黏膜下层剥离时,如果剥离切入黏膜肌层,或是粘膜下层纤维化,剥离过浅,即使是黏膜内癌,但在标本上可能还会存在深部断端有肿瘤残留。这种情况下,临床上所获取的标本,不管是否为黏膜内病变,病理诊断都要判定为VMX。因此,要结合标本与ESD操作的实际情况,进行对照来进行判断(对于剥离过浅的部位,切除后需要观察创面有无病灶残留)。
2)管壁浸润深度
在胃和结肠,要区分是黏膜内癌还是黏膜下层浸润癌。
在胃里,粘膜内癌记为pT1a,黏膜下层浸润癌记为pT1b。
在大肠的黏膜内癌记为pTis,黏膜下层浸润癌为pT1。
另外,根据既往的处理规约,黏膜内癌浸润深度为(m),黏膜下层浸润癌为(sm)。这样的表述,目前还在使用。
食管与胃相同,黏膜内癌为pT1a。黏膜下层浸润癌为pT1b。黏膜内癌进一步又分为
①上皮内癌(pT1a-EP)
②侵及黏膜固有层(pT1a-LPM)
③侵及黏膜肌层(pT1a-MM)
黏膜下层浸润癌,需要区分浅层浸润和深层浸润。对于内镜切除的标本,浸润深度的测量应从黏膜肌层的下缘至癌的浸润先端部垂直测量,根据其数值进行分类(表)。
表 不同脏器管壁浸润深度分类
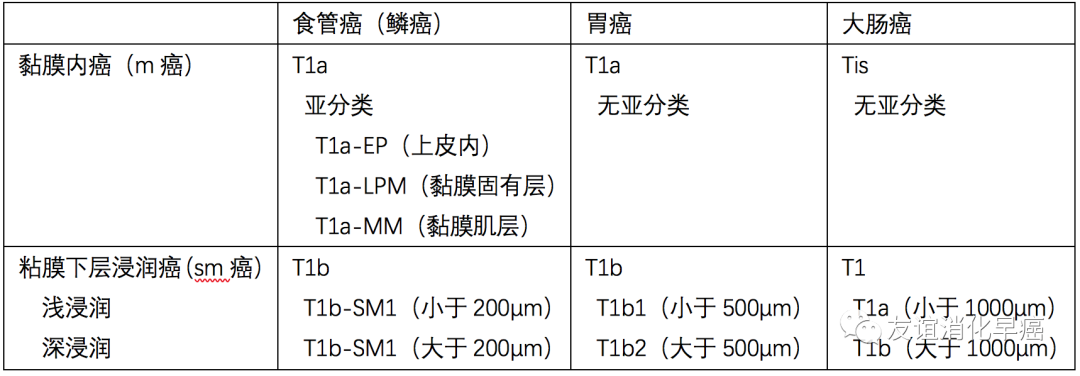
判断不同脏器浸润深度的界值:食管为200μm,胃为500μm,大肠为1000μm。浸润的深浅与淋巴结转移是相关的,对于内镜切除后是否需要追加治疗有指导意义。
大肠的有蒂病变,黏膜肌层错综复杂,不易判断测量的起点,对于这类病例可以分为头部浸润和蒂部浸润,只有蒂部浸润时,才需要测量蒂部浸润的距离。
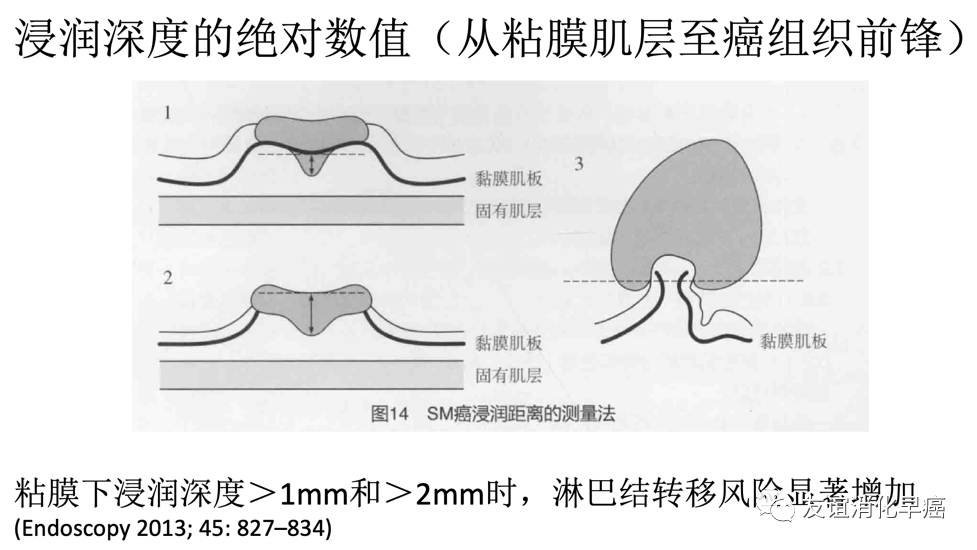
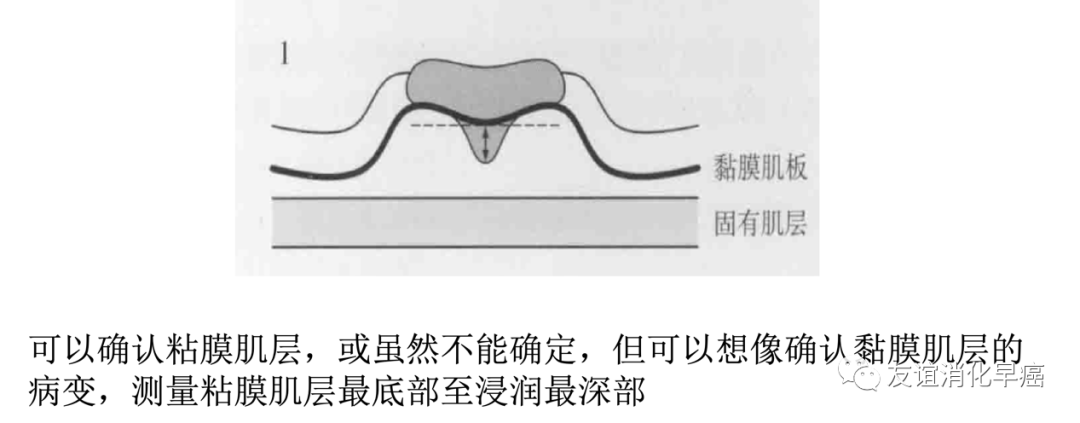
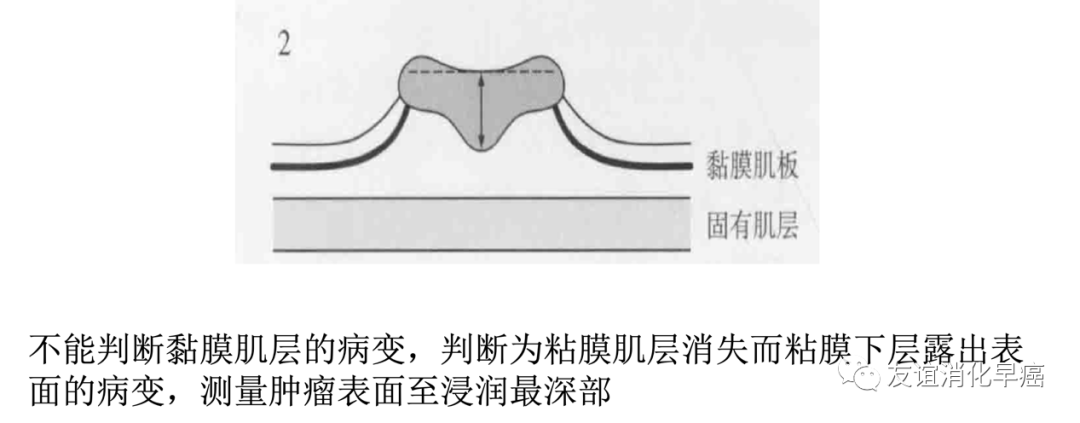
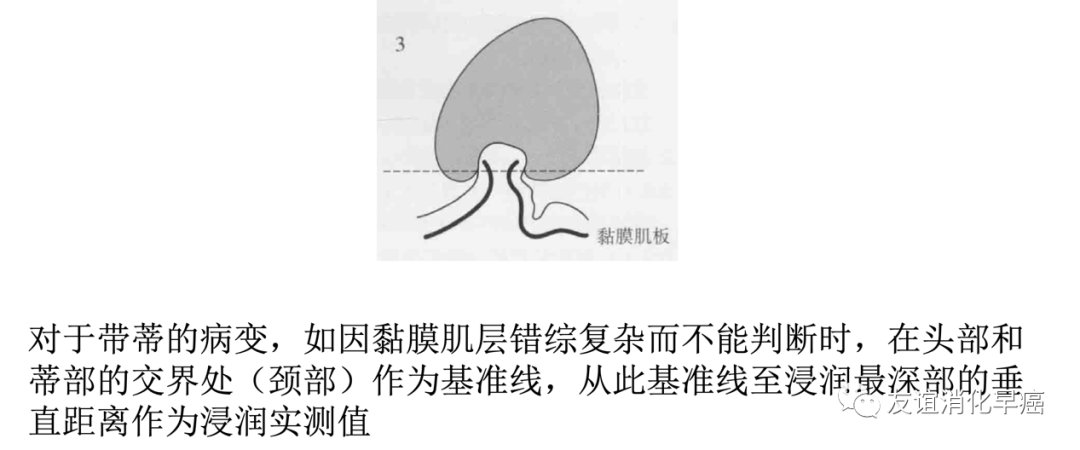
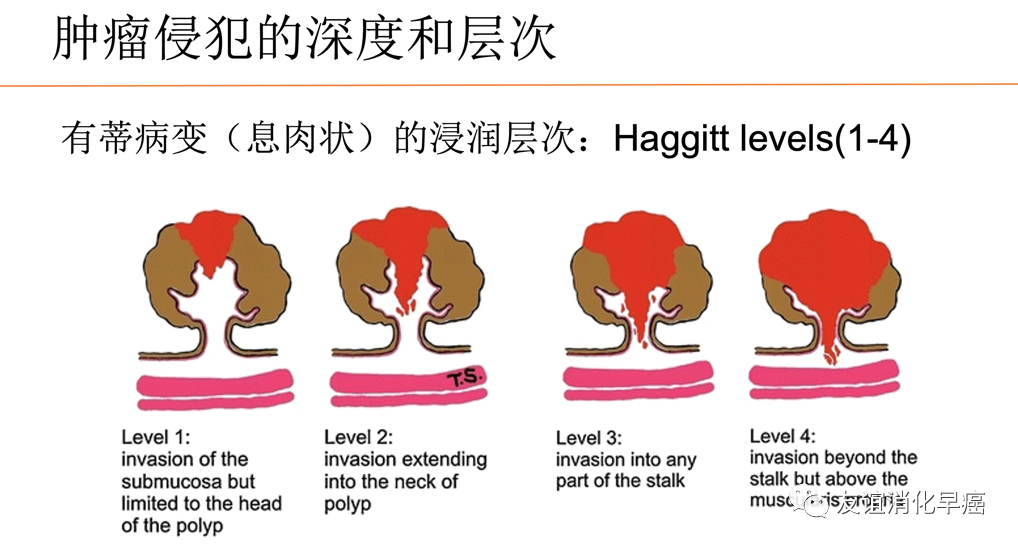
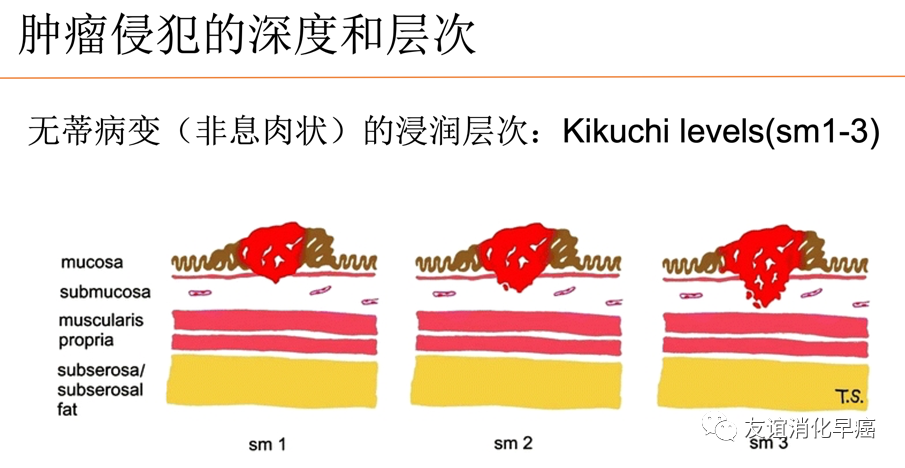
对于判断困难的病例,尤其是依据不同测量方法,浸润深浅会不同时,应当临床和病理之间进行充分讨论。依据不同测量方法,参考不同的结果、最终进行判断。
另外,在进行浸润深度判断时,使用desmin染色可以显示平滑肌,对诊断有帮助。
3)脉管浸润
脉管浸润包括淋巴管浸润和静脉浸润。根据目前的处理规约,淋巴管浸润记为ly。静脉浸润记为v。
淋巴管浸润大多通过HE染色判断。如果诊断明确,可以不进行免疫组化染色。但是,有时内皮细胞和淋巴管腔判断困难时,要进行D2-40免疫组化染色。
静脉浸润的判断则需要进行弹性纤维染色(EVG染色)。内镜切除标本脉管阳性时,有淋巴结转移的风险,应根据患者年龄、既往史、合并症等来综合进行判断,一般建议追加外科手术。
4)浸润方式
根据处理规约,浸润方式进行如下记录。
INFa为膨胀型增殖
INFc为浸润性增殖
INFb 介于两者之间
无论任何脏器,都可能存在主观地判断,评价内镜切除以后是否需要追加治疗的价值目前来说还不是很高。
在食管癌,如果见到固有食管腺导管内的癌非浸润性进展,称为导管内进展。导管内进展并非是浸润性的,没有间质浸润。因此,导管内进展的病灶内,可以见到由柱状上皮组成的内腔,容易判定,有时导管完全被癌组织置换。
癌的膨胀性浸润和脉管浸润难以鉴别。判断困难时,可以进行弹性纤维染色(EVG)、D2-40染色。但是,即使进行这些染色,有时也无法100%判断。对于诊断困难的病例,应该进行临床和病理的沟通,综合考虑是否需要追加治疗。
对于大肠T1癌,要判断浸润的先端部是否有出芽(budding/sprouting)。出芽是指在癌的浸润的先端部可见小的胞巢,单个细胞的浸润,是SM癌淋巴结转移的危险因子。出芽的判断根据HE染色。纤维细胞增生、炎性细胞浸润较重时,不易判断单个癌细胞浸润,癌侵及深部断端附近时,出芽灶由于热变性,判断是否为癌比较困难,此时,可以进行HE染色。CK染色也是有用的。

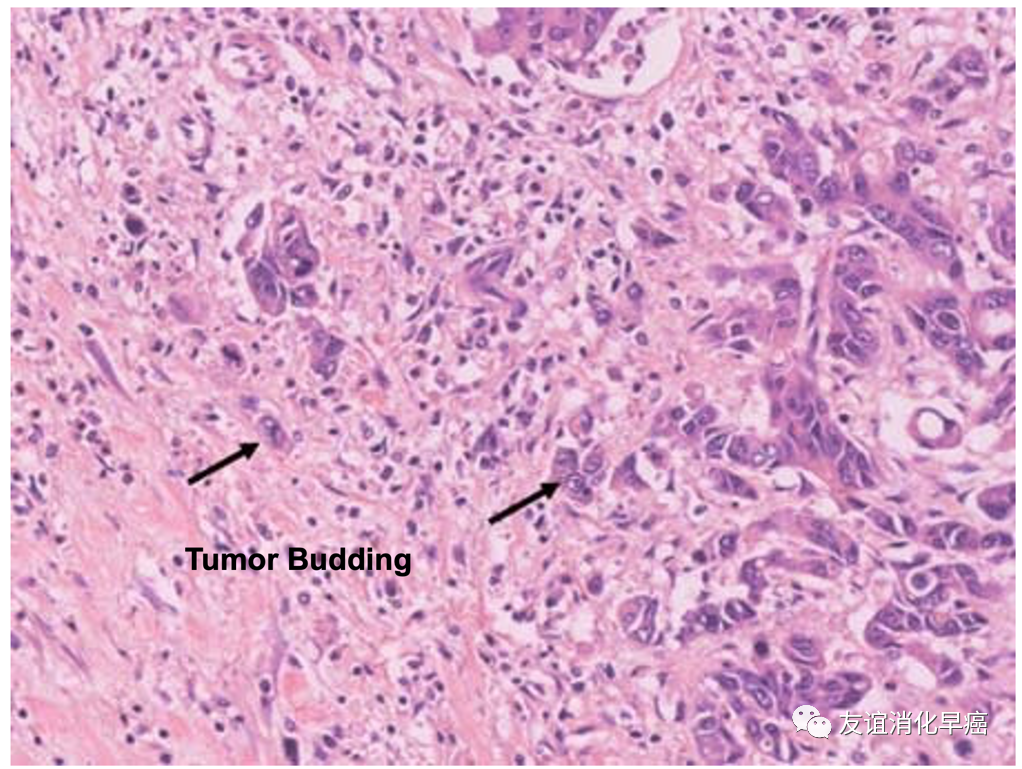
(HE染色)
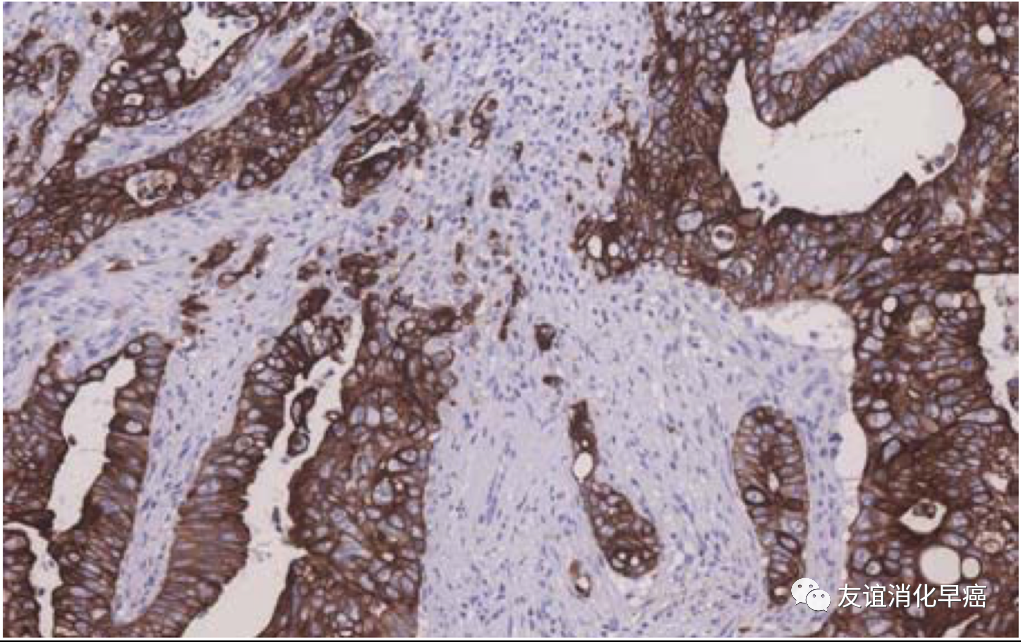
CK染色
5)胃癌内镜切除标本合并溃疡的判断
对于胃癌,是否合并溃疡与内镜治疗后的处理原则是相关的。是否合并溃疡大多通过内镜判断,不同于脉管浸润,后者只能通过病理诊断确定。
溃疡瘢痕的组织像表现为黏膜肌层断裂、交错,黏膜下层纤维化。一般来说,溃疡瘢痕越大,纤维化浸润就越深。纤维下层内见到脂肪组织时,多为活检瘢痕。当然,有时组织学判断也有困难。
判断困难时,根据胃癌治疗指南,参考内镜和消化道造影的图像所见,结合术前是否活检综合判断,决定治疗方案。活检瘢痕和溃疡瘢痕不能区别时,记为UL(+)。
03
结语
本文介绍了从标本处理到病理诊断相关的基础知识,是年轻医生应当掌握的最基础的知识。尽管病理诊断对诊断和治疗有决定作用,但是,也有判断困难的时候。当不能判断时可以进行各种免疫组化染色,即便如此,还有无法判断的情况。由于解释不同,判断结果也会存在差异。因此,有时会用各种符号、文字、数值等进行表示,希望内镜医生能够理解。最后,建立临床医生和病理医生之间的紧密联系是提高双方工作质量的重要途径。